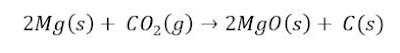Faz uma pesquisa no blogue...
sexta-feira, 10 de setembro de 2010
(ST-RQ) Regras de solubilidade
quinta-feira, 9 de setembro de 2010
(ST-RQ) Reacção de precipitação
(ST-RQ) Reacção de precipitação
Produtos da reacção:
sábado, 4 de julho de 2009
Licor de Fehling
- Dissolver sulfato de cobre(II) pentahidratado em água.
Licor de Fehling B
- Dissolver o tartarato de sódio e potássio e o hidróxido de sódio em água.
Guardar separadamente os frascos do licor de Fehling A e B.
O frasco do licor de Fehling A pode ser de vidro, mas o frasco do licor de Fehling B tem que ser de plástico por causa do hidróxido de sódio.
Usar na proporção de 1:1.
Como preparar?
Um exemplo:
Licor de Fehling A: dissover 69,3g de sulfato de cobre(II) pentahidratado em 1L de água desionizada.
Licor de Fehling B: dissolver 346g de tartarato de sódio e potássio e 50g de hidróxido de sódio em 1L de água desionizada.
quinta-feira, 2 de julho de 2009
quarta-feira, 25 de fevereiro de 2009
quarta-feira, 17 de dezembro de 2008
Química no dia-a-dia...
O que têm as notas de euro?
- Compostos organoestânicos:
*monobutilestanho (MBT);
*dibutilestanho (DBT);
*tributilestanho (TBT).
- P-fenilenodiamina
- Celulose
- Colofónia
- Glutaral (glutaraldeído)
- Sulfato de níquel
Referência bibliográfica:
sexta-feira, 21 de novembro de 2008
quarta-feira, 19 de novembro de 2008
(VMT-CM) Propriedades dos não-metais
- hidrogénio
- azoto
- oxigénio
- flúor
- cloro
- hélio
- néon
- árgon
- crípton
- xénon
- rádon (radão)
O único não-metal que se encontra no estado líquido é o bromo.
Todos os outros não-metais são sólidos à temperatura ambiente.
Os não-metais são considerados maus condutores da corrente eléctrica e do calor.
Contudo, há uma excepção a considerar. A grafite é um bom condutor da corrente eléctrica.
Alótropos do oxigénio
- A molécula de oxigénio é uma molécula diatómica constituída por dois átomos de oxigénio.
- A molécula de ozono é uma molécula triatómica constituída por três átomos de oxigénio.
Destes dois alótropos, o ozono é o menos estável.
Alótropos do carbono
Concatenação do Carbono
Concatenação - ligação entre si de átomos idênticos.
segunda-feira, 17 de novembro de 2008
(VMT-CM) Combustão do magnésio

(VMT-CM) Oxidação do magnésio


No entanto, o magnésio no estado sólido também reage com o dióxido de carbono no estado gasoso, originando para além do óxido de magnésio no estado sólido, o carbono no estado sólido, de acordo com a seguinte equação química:









.jpg)